Sempre più spesso sentiamo parlare di terapie domiciliari per i pazienti covid, ma quali sono? Ad oggi non esiste una cura specifica per SARS-CoV-2, nemmeno in ambito ospedaliero. Per capire come funzionano le terapie disponibili e perché non sono da preferire alla vaccinazione è necessario comprendere, almeno superficialmente, il funzionamento della risposta immunitaria.
L’IMMUNITÀ SPECIFICA
Facciamo qualche passo indietro. Riassumere l’intera immunologia in un paragrafo, per quanto difficile, aiuterà a comprendere quali siano i meccanismi con cui il nostro organismo combatte il covid e dove agiscano le terapie.
Nell’ultimo anno le nostre attenzioni sono state rivolte alla vaccinazione – e non a torto – dal momento che la principale arma che abbiamo per combattere l’infezione è proprio la risposta immunitaria specifica. Questa si articola nella produzione di anticorpi, molecole proteiche definite immunoglobuline (principalmente IgM ed IgG, ma anche IgA), composte da una regione costante, uguale per tutte ed una regione variabile, capace di legarsi in maniera estremamente specifica ad un solo ligando denominato antigene, agendo sia da marcatori che da stimolanti per la risposta immunitaria cellulo-mediata. Le cellule dell’immunità, leucociti come macrofagi e linfociti NK (Natural Killer), a questo punto riconoscono il virus e le cellule infettate da esso (segnalate dagli anticorpi che si legano al virus presente sulla membrana cellulare) ed eliminano entrambi. I macrofagi possono inoltre fungere da APC (Antigen Presenting Cell), inglobando l’antigene, processandolo e mostrandolo ai linfociti T CD8+ citotossici. I linfociti T CD4+ helper hanno invece il compito di stimolare a loro volta le cellule citotossiche ed i linfociti B. Diverse cellule dell’immunità comunicano tra loro, tramite segnali chimici e legami diretti che coinvolgono l’MHC (Major Histocompatibility Complex), insieme di molecole atte a prevenire una risposta immunitaria contro gli antigeni del paziente stesso, che purtroppo può comunque avvenire nel caso di malattie autoimmuni, per diverse cause tra cui la cross-reazione (reazione di un anticorpo con un antigene self, del paziente, diverso da quello che l’anticorpo dovrebbe cercare). L’MHC nell’uomo prende il nome di HLA (Human Leukocyte Antigen) ed è diverso da persona a persona, per questo non è possibile trasfondere i leucociti di un paziente in un altro ancora dotato di sistema immunitario. Nel complesso si avvia la produzione di citochine infiammatorie (TNF, IL-1, IL-6, interferone gamma…) molecole che promuovono l’infiammazione sistemica, generale, caratterizzata da febbre, spossatezza ed altri sintomi. La febbre, definita come una temperatura superiore ai 38 gradi centigradi, aumenta il metabolismo corporeo – da qui la sensazione di stanchezza – e migliora nel complesso l’efficacia della risposta immunitaria.
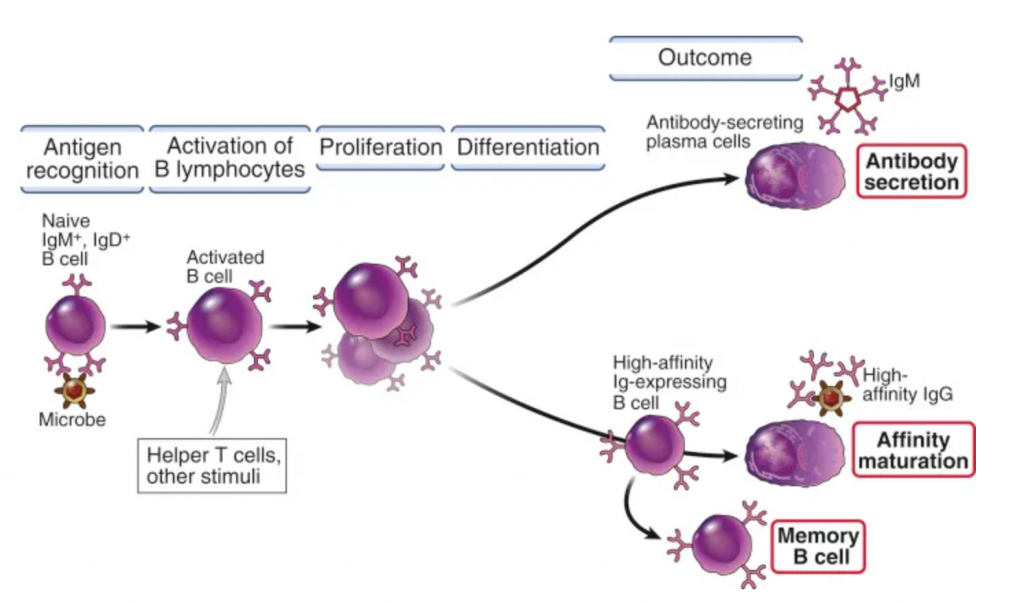
Tutto parte dagli anticorpi, questi sono in grado di riconoscere il virus ed illuminare il bersaglio, ma per essere prodotti necessitano di diverso tempo dal momento dell’infezione, tempo in cui il virus si replica e può iniziare a dare seri problemi, trovando un organismo pressoché incapace di difendersi efficacemente. Le immunoglobuline sono prodotte da un sottoinsieme di leucociti (globuli bianchi) detti linfociti B. Ogni linfocita B produce un solo tipo di anticorpo, definito monoclonale, ovvero una sola serie di copie della stessa identica immunoglobulina, capace di legare lo stesso antigene. Qualora questa, esposta sulla superficie del linfocita, venga a contatto con il rispettivo antigene il linfofcita B naive, che espone un raro tipo di immunoglobuline IgD, si attiva. Viene stimolata la produzione di immunoglobuline IgM ed IgG (per lo stesso identico antigene) ed il distacco delle stesse dalla membrana, nonché la duplicazione della cellula, che genera quindi per mitosi cellule figlie, identiche, a loro volta capaci di produrre la stessa immunoglobulina; che a loro volta saranno stimolate quando entreranno in contatto con l’antigene. Questi linfociti B attivati si trasformano poi in plasmacellule, cellule capaci di produrre grandi quantità di anticorpi monoclonali. Le plasmacellule, una volta eradicata l’infezione, non incontrando più l’antigene tendono a morire, non essendo più stimolate (uno dei tanti feedback negativi che regolano il corpo umano), ma una piccola quantità di cellule B permane (quasi) sempre, per questo vengono definite cellule della memoria. In caso di reinfezione saranno pronte a produrre anticorpi in breve tempo ed a riprodursi.
Le regioni variabili delle immunoglobuline esposte dai linfociti B, che determinano quale antigene attiverà il linfocita, sono sintetizzate in maniera totalmente casuale. Molte di queste sono destinate a legare un antigene con il quale non verremo mai a contatto, altre sono destinate a legare antigeni non pericolosi, scatenando risposte immunitarie – anche violente – assolutamente non necessarie, le allergie; altre ancora sono strutturate per legare un antigene che addirittura non esiste. Per questo dall’infezione può passare molto tempo prima che il linfocita giusto entri in contatto con gli antigeni del coronavirus e si attivi. In questo tempo il virus continua a replicarsi, infettando distretti sempre più ampi e distruggendo le cellule attorno a sé. L’antigene (potenzialmente distribuito in una qualsiasi parte del corpo), viene condotto dallo spazio interstiziale dei tessuti, tramite linfa ed APC, nel sistema linfatico. Per aumentare la probabilità di incontrare l’antigene i linfociti ricircolano nei linfonodi, attratti dalle citochine infiammatorie. Quando lo trovano si attivano e si replicano, ecco perché durante un’infezione i linfonodi, riempiendosi di linfociti, si gonfiano.
I VACCINI
Durante una comune vaccinazione l’antigene, la parte dei una molecola del virus in grado di legarsi ad un anticorpo, stimolando la risposta immunitaria specifica, viene inoculato in maniera controllata, senza che il virus possa replicarsi (virus inattivato), con scarsa probabilità che possa farlo (in vivo attenuato) o tramite una molecola composta da un solo “pezzetto” di virus (a subunità). In questo modo si stimola la produzione di anticorpi senza che il virus possa infettare l’organismo.
I vaccini a vettore virale come Astrazeneca, relativamente moderni, integrano il DNA contenuto in un plasmide (nel caso specifico un adenovirus che infetta lo scimpanzé) con quello di alcune cellule umane destinate poi ad andare in apoptosi (morte controllata), questo viene poi trascritto in RNA e tradotto in una proteina, l’antigene, che andrà a stimolare la risposta immunitaria. Perché non utilizzare un adenovirus umano? Perché sarebbe stato più probabile che la popolazione fosse già entrata in contatto con quell’adenovirus e che di conseguenza avesse avuto il tempo per produrre gli anticorpi atti a contrastarlo, rendendo l’integrazione del plasmide difficoltosa o impossibile: la molecola sarebbe stata attaccata e degradata prima ancora di poter stimolare l’immunità al nuovo coronavirus.
Infine i nuovi vaccini ad mRNA promuovono nei ribosomi la traduzione (assemblaggio della proteina dall’RNA) di frammenti estremamente specifici, come la singola proteina spike che consente a SARS-CoV-2 di legarsi alla membrana cellulare. La proteina stimolerà poi la produzione di anticorpi, ma mancando la restante porzione del virus, compreso l’acido nucleico, sarà impossibile dar luogo ad un’infezione. Il vantaggio di questi ultimi vaccini è che non stimolano immunità nei confronti degli altri componenti del vaccino (come le nanoparticelle lipidiche in cui l’mRNA, molto fragile, è avvolto, necessarie in altre fasi, ad esempio durante l’assorbimento dal sito di iniezione intramuscolare) e di conseguenza consentono di poter modificare la singola porzione di RNA che codifica per l’antigene prodotto, qualora ad esempio il virus dovesse mutare, senza dover produrre de novo un vaccino completamente diverso, risparmiando tempo e denaro.
A lato lo schema di funzionamento di un vaccino anti-covid19 ad mRNA tipo Pfizer Comirnaty o Moderna Spikevax, ad oggi gli unici previsti per la terza dose nei soggetti iper-fragili.

Anche nel caso di pregressa infezione ad oggi è difficile delineare con certezza per quanto tempo le plasmacellule resteranno capaci di riattivarsi. Sappiamo che questo tempo è estremamente variabile da persona a persona e che ci sono svariati casi di reinfezione, dovuti a risposte immunitarie incomplete o poco durature. Per questo la vaccinazione è consigliata anche con sierologico positivo (presenza di anticorpi), concettualmente simile a fare un richiamo. La vaccinazione con i composti approvati dall’EMA garantisce una risposta immunitaria molto solida, di norma molto più della pregressa infezione, ed apparentemente duratura, anche se non è facile nemmeno in questo caso stabilire a priori quanto. A differenza della pregressa infezione sembrerebbe poi garantire un’immunità più larga, capace di contrastare un maggior numero di varianti, ma qui conclusioni definitive sono ancora da trarsi.
LE TERAPIE
Di fronte ad un paziente covid+, non essendoci una terapia specifica, il trattamento riguarda la sintomatologia e le potenziali complicanze della malattia. Va da sé che in presenza di infezione asintomatica non vi sia molto da fare.
L’ivermectina, un farmaco antiparassitario generalmente impiegato nei cavalli, dotato di modesta capacità antivirale, mostrò in uno studio in vitro la capacità di contrastare l’infezione cellulare da SARS-CoV-2. Tuttavia, come spesso accade, la realtà clinica è ben più complessa e l’EMA (come l’AIFA) ne ha sconsigliato l’impiego al di fuori di trial scrupolosamente pianificati. Le dosi necessarie per l’attività antivirale nell’uomo sono infatti molto superiori a quelle generalmente impiegate e può esservi la possibilità, tutt’altro che remota, che il farmaco risulti tossico a dosi efficaci e quindi inutilizzabile.
La terapia sintomatica a domicilio si articola principalmente come antipiretica, volta cioè ad abbassare la febbre. Il paracetamolo, molecola in realtà molto potente nonostante l’immaginario collettivo, è il farmaco di prima scelta. Sorprendentemente per molti il suo meccanismo d’azione non è completamente noto, come quello di molti altri farmaci in commercio. Principalmente inibendo l’enzima cicloossigenasi cox3 riduce la produzione di prostaglandina PGE, responsabile dell’innalzamento della temperatura corporea. TNF, una delle citochine precedentemente citate, induce la febbre proprio stimolando la produzione di prostaglandine. Come ogni pediatra sa, tuttavia, abbassare la febbre – soprattutto quando modesta – non è una via da intraprendere immediatamente, perché come abbiamo visto è durante lo stato febbrile che il sistema immunitario contrasta l’infezione. È quindi consigliabile lasciar decorrere l’infezione, soprattutto in assenza di sintomi particolarmente debilitanti.
Spesso è però proprio lo stato infiammatorio, nel covid come in moltissime altre patologie infettive, a determinare un danno immunomediato, ovvero una flogosi importante sostenuta da una risposta immunitaria eccessiva e poco specifica, che distrugge i tessuti sani, in questo caso prevalentemente il parenchima polmonare. Il cortisone ed altri steroidi sono da somministrare solo in presenza di forte sintomatologia respiratoria, per ridurre l’infiammazione. Somministrati precocemente, ad esempio a domicilio, non solo non servono, ma possono risultare dannosi, andando a inibire anche un’adeguata risposta immunitaria ed aumentando la capacità del virus di replicarsi, infettando e distruggendo le cellule sane.
In presenza di infezione, delle basse e delle alte vie aeree, è prassi poco diffusa, ma fin troppo comune, somministrare un antibiotico ad ampio spettro, contravvenendo alle più moderne linee guida dell’ISS. Se in una stretta minoranza di casi un’infezione batterica si può sovrapporre all’infezione da coronavirus – e quindi la sintomatologia regredisce somministrando l’antibiotico – nella stragrande maggioranza dei casi l’antibiotico non occorre. Prescriverlo significa andare a promuovere la selezione di ceppi resistenti di batteri, questione a cui l’OMS volge primaria attenzione, ormai arci-nota anche ai non addetti ai lavori. Il rischio di tornare in futuro ad un’era pre-antibiotica non è poi così remoto, soprattutto se in tutto il mondo si cominciassero a prescrivere di default antibiotici ad ogni paziente covid. Già oggi esistono, ceppi di batteri resistenti a qualsiasi antibiotico conosciuto, fortunatamente non sempre sono pericolosi per una persona con un sistema immunitario efficiente, ma da essi se ne possono generare di più aggressivi. Questi si concentrano anche nelle strutture ospedaliere, dove il largo impiego di antibiotici e il continuo turn over di pazienti aumentano le possibilità di selezionare un ceppo resistente.
L’infiammazione coinvolge anche alcuni componenti del sangue definiti complemento. Queste molecole si ricombinano tra loro attraverso una complessa catena enzimatica, oltre ad avere un ruolo nell’attivazione dell’immunità specifica, promuovono la coagulazione. La malattia da SARS-CoV-2 può poi svilupparsi anche in una forma simil-vasculitica, che interessa la parete dei vasi sanguigni. La somministrazione di antitrombotici a dosi profilattiche può essere valutata a domicilio, dopo attenta analisi del quadro clinico: soprattutto negli anziani il rischio di complicanze emorragiche dovute ad una scarsa coagulazione sono estremamente frequenti. L’eparina, anticoagulante, è ormai sempre presente a dosi profilattiche (basse) nel contesto ospedaliero.
Se il quadro peggiora è necessario il ricovero, dove il paziente viene continuamente monitorato, con esami di laboratorio e strumentali. Sotto questa attenta osservazione si può procedere con l’attuale terapia di supporto, da calibrare adeguatamente ed aggiornare quotidianamente, che si basa su tre principi cardine: cortisonici o corticosteroidi ad alte dosi (anti-infiammatori) per vena e decalage fino alla somministrazione per bocca in caso di miglioramento, eparina a basse dosi e ossigenoterapia: dagli alti flussi (senza eccedere, perché gli atti respiratori, soprattutto nell’anziano, sono stimolati anche dalla carenza di ossigeno), NIV (Non Invasive Ventilation) ovvero casco/maschera con ossigeno e ventilazione meccanica e, nei casi più gravi, intubazione. Anche di fronte ai quadri prognostici peggiori quindi, la strategia non è al momento volta a contrastare direttamente il virus, non essendo possibile in mancanza di una terapia specifica, ma ad arginare l’ingente risposta immunitaria aspecifica nell’attesa dello sviluppo di una risposta umorale specifica, anticorpo-mediata, che possa risolvere l’infezione, mentre si lavora per garantire i parametri vitali del paziente.
Farmaci come l’idrossiclorochina, che si ipotizzava potessero contrastare la replicazione virale, non hanno prodotto evidenze positive negli studi caso-controllo.
Infine, grande sforzo è stato destinato allo sviluppo di farmaci con attività antivirale ad uso orale. Attualmente Merck e Pfizer sono le case farmaceutiche che hanno presentato risultati più avanzati nelle fasi di ricerca. Nessun farmaco di questo tipo è stato ancora approvato dall’EMA o dall’FDA, ma alcune richieste sono al vaglio proprio in questi giorni.
I famosi anticorpi monoclonali
Spesso abbiamo sentito poi parlare di anticorpi monoclonali, quasi esclusivamente in maniera impropria e superficiale. L’argomento è vasto e complesso, tali anticorpi sono utilizzati sia in ambito diagnostico che terapeutico, ma raramente si fa riferimento ad anticorpi anticovid.
Le biotecnologie e l’ingegneria genetica hanno consentito negli scorsi decenni di creare farmaci estremamente specifici, sfruttando la specificità degli anticorpi. In vitro, da linee cellulari (non necessariamente umane) immortalizzate è oggi possibile ottenere immunoglobuline particolarmente utili. Una di queste ha come antigene il recettore di IL-6, una delle citochine dell’infiammazione precedentemente citate. L’anticorpo al recettore di IL-6 occupa il sito di legame senza provocare l’attivazione del dominio citoplasmatico (tappa il sito senza accenderlo), prevenendo il legame di IL-6 con il suo recettore e inibendo l’azione dell’interleuchina, riducendo l’infiammazione. Il farmaco è entrato in commercio nel 2013 con il nome di Tocilizumab, una molecola potente e non scevra di effetti collaterali, anche gravi, come infezioni delle alte vie aeree e disfunzioni renali. Tutti i farmaci che finiscono per MAB sono anticorpi monoclonali (Monoclonal Anti-Body). Possono dividersi in quelli che finiscono per UMAB, anticorpi monoclonali derivati da cellule umane; XIMAB, chimerici (regione variabile animale, regione costante umana); ZUMAB, umanizzati (derivati principalmente da cellule umane) e OMAB, murini (derivati da cellule di topi da laboratorio).
Gli anticorpi monoclonali sono largamente impiegati anche nella diagnostica pura, attraverso le tecniche di ricerca dell’antigene, come nei test di gravidanza o nell’analisi dei marker tumorali, dove l’anticorpo legandosi ad una specifica proteina ne segnala la presenza. Anche alcuni tamponi covid vengono analizzati tramite tecniche di immunofluorescenza, dove alla regione costante dell’anticorpo è legato un micro-pigmento fluorescente. In caso di positività gli anticorpi si addensano attorno ad un area del materiale prelevato dalla mucosa rinofaringea con il tampone e disposto in vetrino. La luce appare visibile ad occhio nudo o tramite apposita strumentazione. Persino i test sierologici rapidi, atti a valutare la presenza di anticorpi, IgG o IgM, anti-SARS-CoV-2, sfruttano a loro volta gli anticorpi monoclonali, essendo di norma basati sulla tecnica immunoenzimatica (ELISA). Si punge il dito e lo si mette a contatto con il kit. L´antigene del coronavirus, che è contenuto nel kit, si lega alle immunoglobuline specifiche eventualmente precedentemente prodotte dal paziente e circolanti nel sangue. Dopo i lavaggi per eliminare gli anticorpi che non si sono legati all’antigene fissato sul substrato del kit, si aggiungono gli anticorpi monoclonali anti-umani (ovvero capaci di legare la propria regione variabile la regione costante dell’anticorpo umano), anti-IgA/IgM/IgG anticovid. L’avvenuto legame tra anticorpo anticovid del paziente e l´anticorpo antiumano fa si che la soluzione attivi un enzima, che processando un reagente consente di sviluppare un colore o una fluorescenza.
Se all’anticorpo invece dell’enzima è legato un radionuclide (in genere Iodio 125) si parla di RIA (Radio Immuno Assay) e la positività si misura dalla radioattività espressa. Ad ogni test è associato un valore percentuale di specificità, la capacità dell’anticorpo di legarsi ad un antigene senza confonderlo con qualcos’altro dando un falso positivo, e sensibilità, la capacità dell’anticorpo di legarsi ad una piccola quantità di antigene senza ignorarla dando un falso negativo. I test di screening tendono in genere ad essere progettati per prendere più positivi possibile, cercando di comprendere le code positive della gaussiana, generando non pochi falsi positivi, ovvero casi che saranno giudicati negativi da un test di secondo livello, più approfondito.
Infine di anticorpi monoclonali si parla anche quando si presuppone la somministrazione diretta per via endovenosa di anticorpi anticovid a scopo terapeutico. I farmaci citati in genere sono il bamlanivimab ed l’etesevimab, che ad oggi tuttavia non hanno fornito nei trial evidenze particolarmente incoraggianti. La somministrazione di anticorpi in vena non è scevra di rischi, anzitutto relativi alle reazioni allergiche e poi trombotici (ben superiori a quelli della vaccinazione), essendo come detto l’infiammazione associata alla coagulazione ed essendo l’infusione continua intravenosa possibile causa di lesioni alle pareti venose. Il rischio è la trombo-embolia: da una trombosi venosa degli arti inferiori (a cui sono più soggetti i pazienti ospedalizzati, allettati) si stacchi un frammento, un embolo, che condotto dal torrente ematico giunga per vasi di calibro via via superiore all’atrio destro, al ventricolo destro e quindi passate le arterie polmonari vada ad incunearsi nella sempre più ramificata circolazione arteriosa polmonare, impedendo il corretto afflusso di sangue con conseguente aumento dello spazio morto (volume polmonare non soggetto a scambi gassosi) aggravando la patologia respiratoria. Il 16 aprile 2021 la FDA ha ritirato l’autorizzazione d’emergenza per il bamlanivinab perché si evinsero rischi superiori ai benefici.
Restano poi le problematiche relative all’infusione di qualsiasi anticorpo monoclonale, che è fattibile solo in ambiente ospedaliero, sotto stretto controllo medico, che non sempre è risolutiva (perché non sempre gli anticorpi riescono ad attivare efficacemente l’immunità cellulo-mediata) e che non è mai capace di conferire un’immunità duratura, dal momento che non crea plasmacellule capaci di produrre anticorpi e che gli anticorpi infusi finiscono col degradarsi progressivamente, esponendo quindi a reinfezione il paziente e aumentando le possibilità di un nuovo ricovero. In compenso occupa parecchie risorse ospedaliere, umane e tecnologiche, oltre che logistiche. Non può rappresentare ad oggi il metodo d’elezione per la cura dei pazienti covid. Discorso pressoché analogo per il plasma iperimmune, cui si aggiunge anche la necessità d’estrazione dal donatore immunizzato.
In conclusione
Le terapie sintomatiche e di supporto sono svariate e funzionano discretamente, come confermato dalla riduzione della mortalità ospedaliera rispetto ai primi mesi di pandemia, anche tra i non vaccinati. I farmaci potenzialmente impiegabili sono molti, l’AIFA ne ha stilato una nutrita lista in costante aggiornamento e ha recentemente autorizzato svariati trial, ad esempio con sartani ed ACE-inibitori, farmaci anti-ipertensivi che potrebbero aiutare a prevenire le complicanze della malattia inseriti in un protocollo terapeutico ampio.
Risulta tuttavia di fondamentale importanza ribadire che nel complesso quadro di manifestazione della patologia non esiste ad oggi una terapia specifica e mirata, né ospedaliera né tanto meno domiciliare. Non può che destare perplessità l’apprendere che in Senato, dal 12 al 14 settembre, si sia tenuto un convegno al riguardo, organizzato dalla senatrice Ferrero (Lega), al quale hanno per altro partecipato come relatori figure controverse, caratterizzate da una lunga storia d’attrito con le più prestigiose istituzioni medico-scientifiche.
L’orientamento terapeutico è oggi ancora volto a concedere all’organismo il tempo necessario per sviluppare una efficiente risposta immunitaria umorale (anticorpo-mediata). Risposta che il vaccino sappiamo già per certo indurre efficacemente nella quasi totalità dei pazienti.



1 comment